新型冠状病毒(SARS-CoV-2)引起的疫情仍在持续,据世界卫生组织官网显示,截至2023年1月8日,全球已报告确诊病例超过
6.59亿例 660万例
由于新冠病毒持续累积突变,免疫逃逸能力越来越强,导致人们在接种病毒后仍会出现感染现象。
如何提前预测病毒的进化轨迹,成为研究人员在下一代疫苗设计中需要攻克的难题!
鉴于此,
武汉大学病毒学国家重点实验室蓝柯教授和徐可教授团队通过追踪新冠病毒的进化轨迹,
设计出一种新型新冠广谱疫苗 Science Translatio
Vaccination with Span, an antigen guided by SARS-CoV-2 S protein evolution, protects against challenge with viral variants in mice。
2020年4月,新冠病毒流行之初,该团队就开始了这项课题攻关,提出了
“ 基于病毒进化共识序列,优化设计疫苗免疫原”
并且首次提出
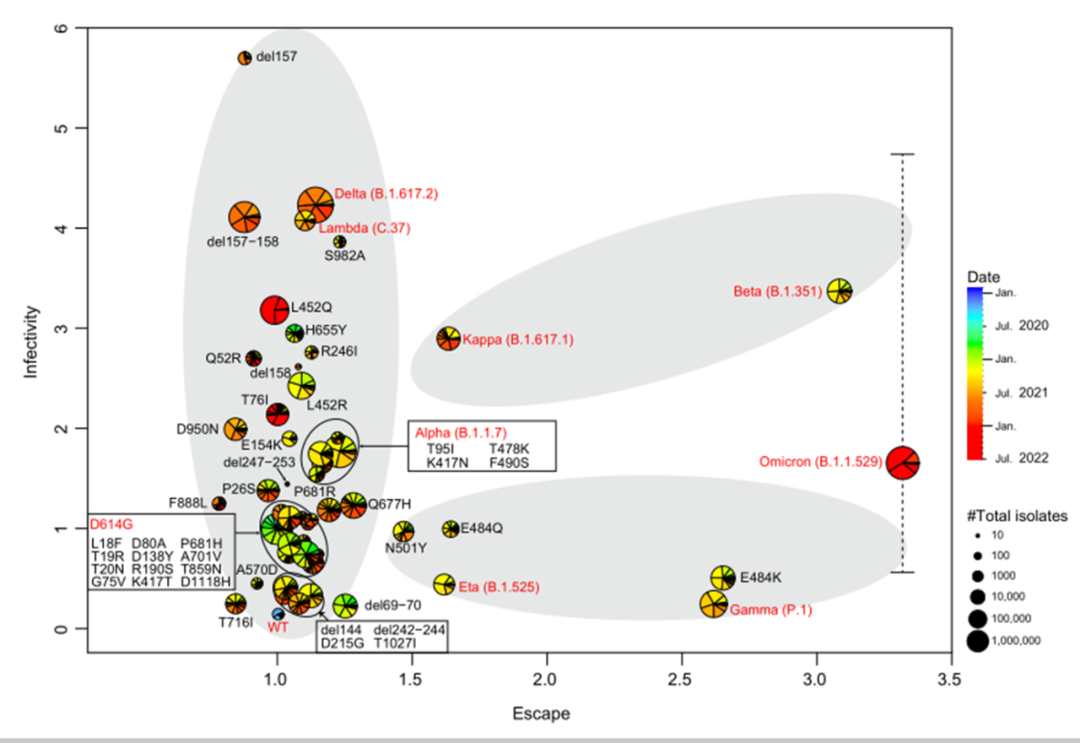
新冠病毒的进化路径
新冠病毒刺突(Spike,S)蛋白的突变并不是完全随机的,而是沿着三条定向路径进化。
其中一条路径是突变导致高细胞感染性的同时保持弱的免疫逃逸能力(如Delta株和Lambda株);第二条路径是突变导致低细胞感染性的同时获得强免疫逃逸能力(如Gamma株);第三条路径的变异株数量相对较少,它们的细胞感染性和免疫逃逸能力同时增强(如Beta株)。这说明在大多数情况下,S蛋白的突变对功能的调控需要协调,而不是简单的增强或减弱。
新冠病毒为什么凶猛?一个重要原因就是病毒不断的变异,难以交叉免疫的原因也就在于此。
羊了一回,免疫系统产生了抗体,但是这个抗体只是针对感染的毒株,换一种新毒株,免疫系统就很难认出来了。
很多新冠变病毒异株的突刺蛋白相对初期流行的毒株,变异点位已经多达十几个甚至几十个。而人体的免疫系统构建屏障和抗体的核心就是病毒突刺蛋白的氨基酸结构。
由于毒株变异太快,免疫系统的计划赶不上变化,往往导致好不容易合成的抗体的效力大大减弱。
病毒变异再快,变的部分总是少数,不变的部分总是多数。能不能结合之前的数据,参考那些没变的部分,造一个人造抗原出来,然后教免疫系统认得这个抗原。
按照这个思路,造出来的人造抗原代表了大批变异病毒的共同特征。说白了,有点万变不离其宗的意思,以后就不怕认不出来了。
然后再通过这个人造抗原进行动物实验,争取让动物的免疫系统产生能对绝大多数变异毒株都有效的抗体。
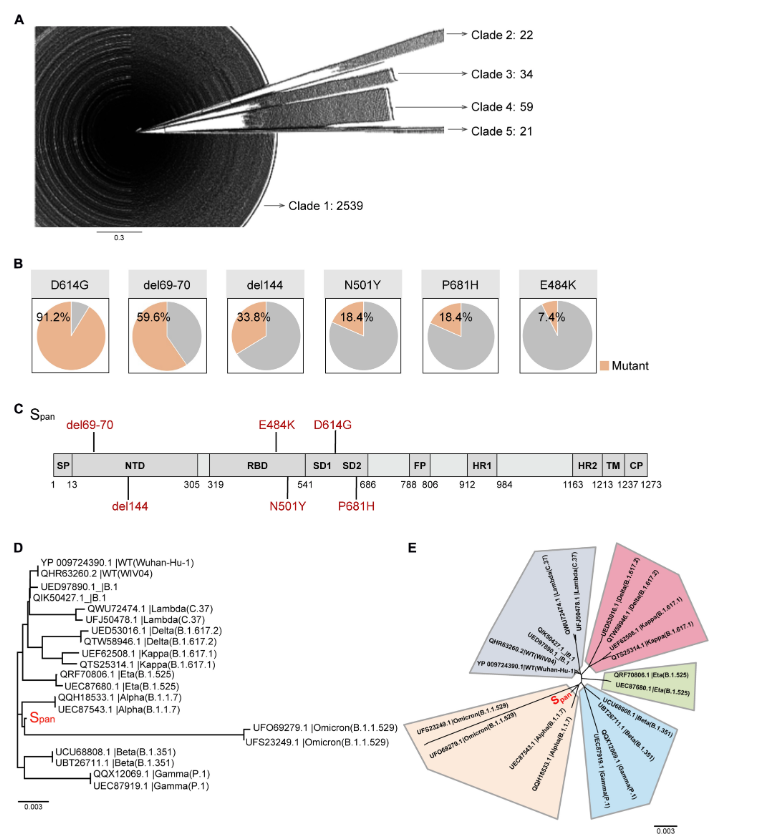
研究人员通过数据比对,下载了截至2021年2月NCBI数据库中所有新冠病毒序列,去重后获得2675条序列,通过进化聚类算法,计算分析得出共性突变位点和进化规律,设计出了人造抗原Span。
论文作者之一徐可表示:可以说,它是新冠病毒毒株中最有代表性、最普适的一条序列。就像一个家庭里有数个兄弟姐妹,我们找出他们的共同特征并集中到了一起。
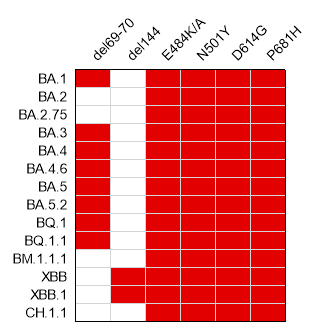
武大团队发现的6个共性突变位点在Omicron流行株(纵向标记)中均有很大程度的保留(红色表示该位点保留)。
Span抗原的6个共性突变位点在奥密克戎流行株中均有很大程度的保留,最近备受关注的新毒株BQ.1、BQ.1.1和XBB、XBB.1,包括在美国强势崛起的XBB.1.5,也都和Span抗原共享5个共性突变位点。
研究显示,Span抗原序列恰好位于新冠病毒S蛋白系统发育树的中心位置,而且和奥密克戎聚类到一起。
许可教授在接受记者采访时坦言,“
这款疫苗有别于传统的单序列疫苗,有着较大的概念性创新,从本质上提升了抗原的广谱性。
我们还会持续追踪病毒在真实世界的变异,但采用这种方式做出的广谱疫苗,比过去我们追着病毒跑已经好了很多,走到了病毒的前面。
未来或许五年或十年打一针广谱疫苗就够了
版权申明
汽轮机冲转暖机结束的标志到底是什么 汽轮机的启动是一个不稳定的加热过程,进行合理经济的启动就是寻求合理的加热方式,使启动过程中机组各部分热应力、热变形、胀差
0评论 2023-02-07 580
天体物理理解的进步 以下文章来源于中国科学院理论物理研究所
,作者韩超中国科学院理论物理研究所
.
理论物理所科研动态和综合新闻的发布;理
0评论 2023-02-07 344